- English
- Español
- Português
- русский
- Français
- 日本語
- Deutsch
- tiếng Việt
- Italiano
- Nederlands
- ภาษาไทย
- Polski
- 한국어
- Svenska
- magyar
- Malay
- বাংলা ভাষার
- Dansk
- Suomi
- हिन्दी
- Pilipino
- Türkçe
- Gaeilge
- العربية
- Indonesia
- Norsk
- تمل
- český
- ελληνικά
- український
- Javanese
- فارسی
- தமிழ்
- తెలుగు
- नेपाली
- Burmese
- български
- ລາວ
- Latine
- Қазақша
- Euskal
- Azərbaycan
- Slovenský jazyk
- Македонски
- Lietuvos
- Eesti Keel
- Română
- Slovenski
- मराठी
- Srpski језик
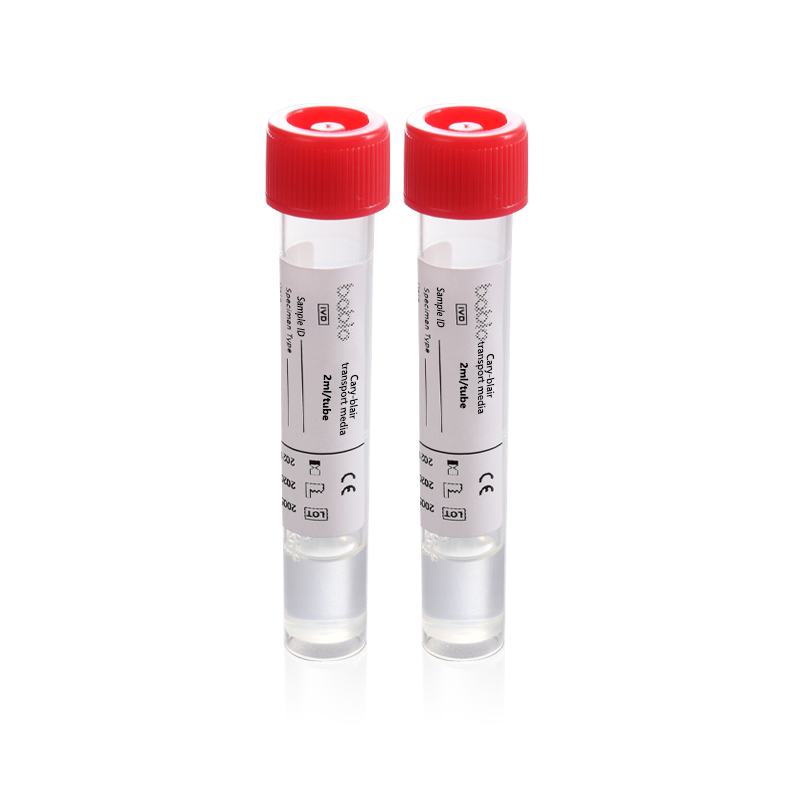
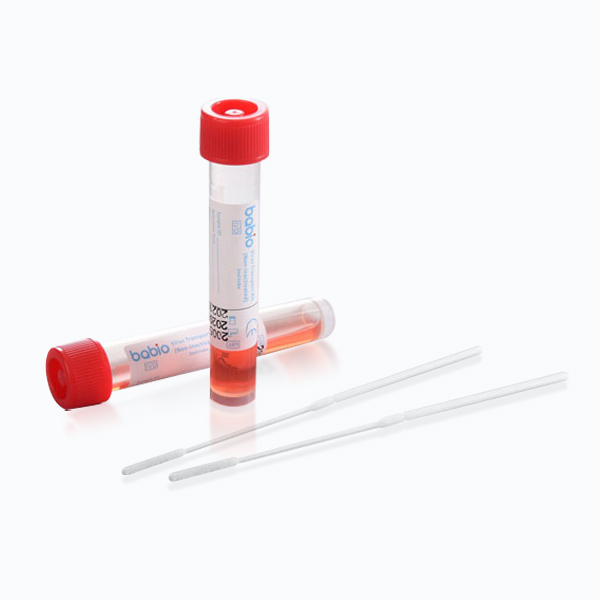
Support de transport Cary-Blair modifié
Le milieu de transport Cary-Blair modifié est recommandé pour la collecte et l’expédition d’échantillons cliniques.
envoyer une demande
UTILISATION PRÉVUE
Cary-Blair Transport Media est recommandé pour la collecte et l’expédition d’échantillons cliniques.
RÉSUMÉ ET EXPLICATION
Les infections entériques peuvent être causées par différents types de bactéries. Compte tenu d'un si large éventail d'agents pathogènes et de la nécessité de limiter les coûts, la contribution des médecins et les directives de pratique peuvent aider le laboratoire à déterminer quels tests sont appropriés pour détecter l'agent étiologique de la diarrhée. Les laboratoires de microbiologie devraient examiner l'épidémiologie locale de l'entérocolite bactérienne et mettre en œuvre des méthodes de culture de selles de routine qui permettront la récupération et la détection de tous les principaux agents pathogènes responsables de la plupart des cas dans leur zone géographique. Tous les laboratoires de microbiologie doivent régulièrement tester la présence de Salmonella spp, Shigella spp et Campylobacter spp. sur toutes les cultures de selles.1 L'une des procédures de routine dans le diagnostic des infections entériques implique la collecte et le transport en toute sécurité d'échantillons sur écouvillon rectal ou d'échantillons de selles. Ceci peut être accompli en utilisant le support de transport Cary-Blair modifié. Le milieu est conçu pour maintenir la viabilité des bactéries entériques pathogènes pendant le transit vers le laboratoire d'essais.
PRINCIPES DE LA PROCÉDURE
Ce milieu ne contient aucun composant nutritionnel, permettant la conservation des spécimens dans un état non nutritif pendant une période prolongée. La présence de thiogycollate de sodium dans le milieu crée un environnement à faible potentiel d'oxydo-réduction,
L'hydrogénophosphate disodique agit comme un tampon et le chlorure de sodium maintient l'équilibre de la pression osmotique du système et régule également la perméabilité de la membrane cellulaire bactérienne.
STOCKAGE
Ce produit est prêt à l’emploi et aucune préparation supplémentaire n’est nécessaire. Le produit peut être scellé et stocké à 2-25 ℃ pendant 18 mois jusqu'à son utilisation. Ne surchauffez pas. Ne pas incuber ni congeler avant utilisation. Un stockage inapproprié entraînera une perte d’efficacité. Ne pas utiliser après la date de péremption.
DÉTÉRIORATION DU PRODUIT
Le milieu de transport Cary-Blair modifié ne doit pas être utilisé si (1) il existe des preuves de dommages ou de contamination du produit, (2)
il y a des signes de fuite, (3) la date de péremption est dépassée, (4) l'emballage est ouvert ou (5) il y a d'autres signes de détérioration.
DATE D'EXPIRATION
18 mois à compter de la date de fabrication.
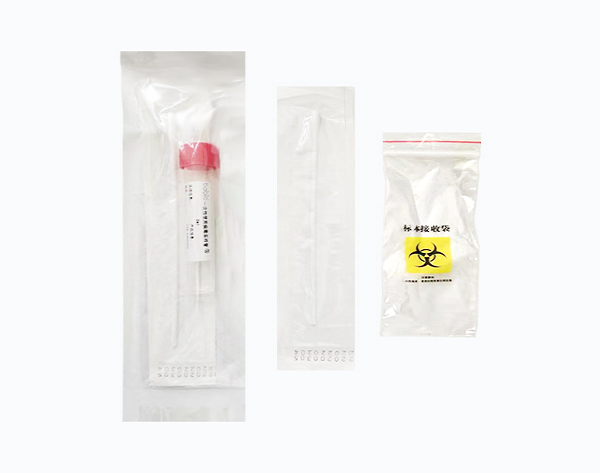
COLLECTION D'ÉCHANTILLONS
Échantillons sur écouvillon rectal et échantillons de selles collectés pour des analyses microbiologiques qui comprennent l'isolement des substances entériques
les bactéries pathogènes doivent être collectées et manipulées conformément aux manuels et directives publiés.1,7-10 Pour maintenir un niveau optimal
viabilité de l'organisme, transporter les échantillons collectés à l'aide du milieu de transport Cary-Blair modifié directement au laboratoire, de préférence dans les 2 heures suivant le prélèvement.1,7-12 Si la livraison ou le traitement immédiat est retardé, les échantillons doivent être conservés à 2-8 °C et traité dans les 24 heures.
Les exigences spécifiques concernant l'expédition et la manipulation des échantillons doivent être entièrement conformes aux réglementations locales.3-6L'expédition des échantillons au sein des établissements médicaux doit être conforme aux directives internes de l'établissement. Tous les échantillons doivent être traités dès leur réception au laboratoire.
PROCÉDURES
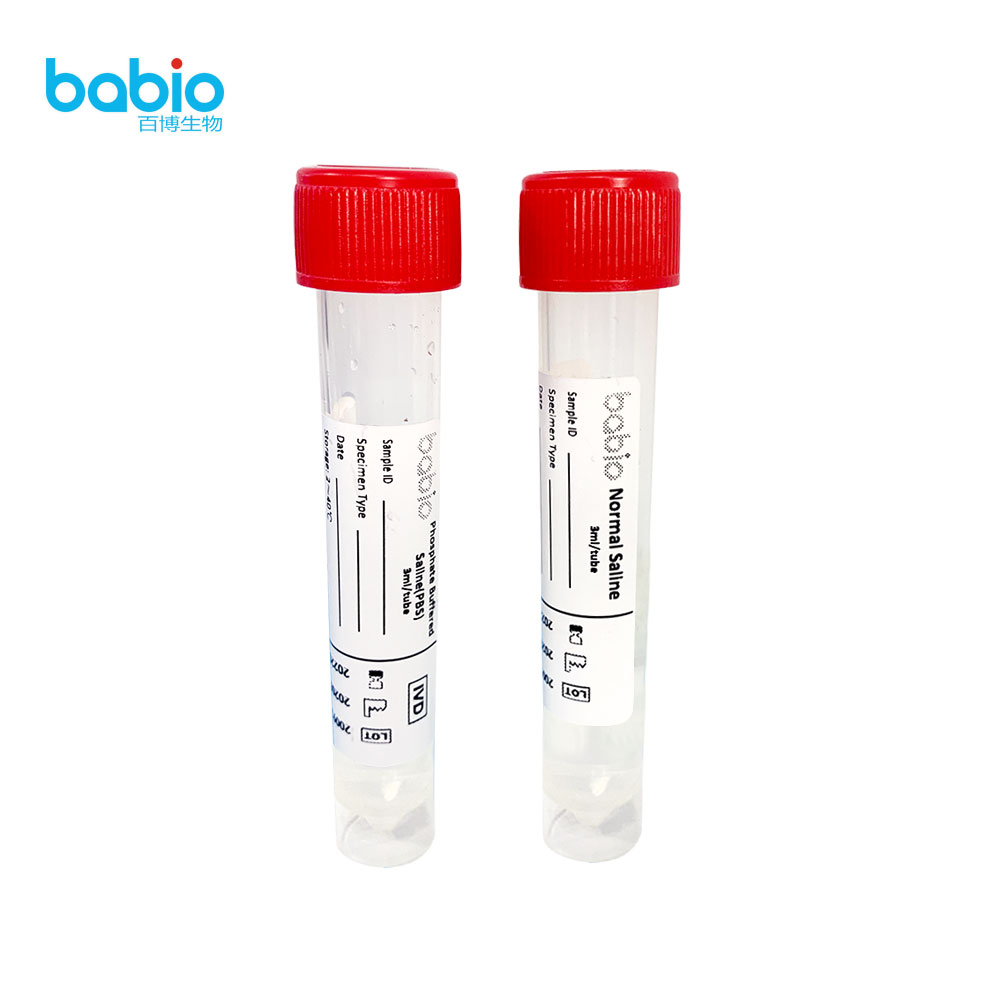
Matériel fourni : Tube à bouchon à vis en polypropylène rempli de 2 ml ou 3 ml de milieu de transport Cary-Blair modifié. Spécifications : 2 ml/tube, 3 ml/tube ; 20 pièces/paquet, 50 pièces/paquet, 100 pièces/paquet.
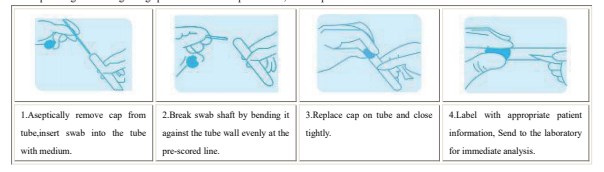
Procédure de testa
Un prélèvement approprié d’échantillons sur le patient est extrêmement essentiel pour réussir l’isolement et l’identification des organismes infectieux.
Pour obtenir des conseils spécifiques concernant les procédures de prélèvement d’échantillons, consultez les manuels de référence publiés.
CONTRÔLE DE QUALITÉ
Les applicateurs de milieux de transport Cary-Blair modifiés sont testés pour garantir qu'ils sont non toxiques pour les bactéries pathogènes entériques. Le milieu de transport Cary-Blair modifié BPX® est testé pour la stabilité du pH. BPX®Modified Cary-Blair Transport Media est un contrôle qualité
testé avant sa commercialisation pour vérifier sa capacité à maintenir des bactéries pathogènes entériques viables à température ambiante pendant des périodes spécifiées. Si des résultats de contrôle qualité aberrants sont constatés, les résultats des patients ne doivent pas être communiqués.
LIMITES DE LA PROCÉDURE
1. L'état, le moment et le volume des échantillons collectés pour la culture sont des variables importantes pour obtenir des résultats de culture fiables. Suivez les directives recommandées pour la collecte d’échantillons.
2. Ce produit est destiné à être utilisé avec les écouvillons. L'utilisation de tubes de milieu ou d'écouvillons provenant de toute autre source n'a pas été validée et pourrait affecter les performances du produit.
3. Dans le laboratoire, portez des gants en latex et autres protections proportionnées aux précautions universelles lors de la manipulation des échantillons cliniques.
4. Le milieu de transport Cary-Blair modifié est destiné à être utilisé comme milieu de collecte et de transport pour les bactéries entériques pathogènes. Le milieu de transport BPX®Modified Cary-Blair ne peut pas être utilisé comme milieu d’enrichissement, sélectif ou différentiel.
PERFORMANCE
Dans un environnement aseptique, à l'aide d'un écouvillon pour prélever des échantillons de Vibrio parahaemolyticus, Salmonella enterica et Shigella flexneri, conservez-les à 20-25°C pendant 48 heures. Transférez ensuite les échantillons sur un milieu gélose au sang et incubez à 36 ± 1 ° C pendant 18 à 24 heures pour observer la viabilité bactérienne. Les bactéries devraient bien se développer.